1. Le modèle SIR fondamental [février 2025]
Méthodologie
Cette étude présente une analyse complète du modèle SIR (Susceptible-Infectious-Removed) avec résolution numérique des équations différentielles et analyse des nullclines.
Les trois compartiments
Le modèle SIR classique divise la population en trois compartiments :
- S (Susceptibles) : individus non immunisés, pouvant être contaminés
- I (Infectieux) : porteurs de la maladie, contaminant les susceptibles
- R (Retirés) : immunisés (après guérison) ou décédés
où N est la population totale, et $, $, $ les effectifs de chaque compartiment.
Équations du modèle
La transmission de la maladie est modélisée par un terme d'action de masse :
où β est le taux de transmission. La force d'infection est définie par λ = β I.
Soit τ la période infectieuse, alors le taux de guérison est γ = 1/τ.
avec :
- μ : taux de natalité
- δ : taux de mortalité (souvent δ = μ pour population constante)
- γ : taux de guérison
- β : taux de transmission
Nombre de reproduction de base R₀
Un individu infectieux contamine en moyenne β personnes par unité de temps pendant une durée τ, soit :
Ce paramètre fondamental détermine le comportement de l'épidémie :
- R₀ < 1 : l'épidémie s'éteint
- R₀ > 1 : l'épidémie se propage
- R₀ = 1 : seuil critique
Impact du nombre de reproduction de base R₀ sur la sévérité de l'épidémie
_beta.0.7_gamma.0.2_mu.0.png)
Évolution temporelle des trois compartiments : Susceptibles (S), Infectés (I), Retirés (R)
Lorsque l'épidémie démarre, la fraction d'infectés I(t) croît de manière exponentielle avec un taux de croissance initial donné par r = γ (R₀ - 1). Plus R₀ est élevé, plus la croissance initiale est rapide et plus l'épidémie sera sévère. Pour des valeurs de R₀ typiques (2 à 3 pour la grippe, 3 à 5 pour le COVID-19), on observe une croissance rapide du nombre d'infectés, soulignant l'importance de mesures de contrôle pour réduire R₀ en dessous de 1. On remarque également que la fraction finale de la population touchée par l'épidémie (R*) est une fonction croissante de R₀, avec une transition rapide autour de R₀ = 1. Cette fraction ne vaut pas systématiquement 1 même pour des R₀ élevés, en raison de l'immunité collective qui se développe au fur et à mesure que les individus passent dans le compartiment R. Lorsque le nombre de susceptibles S(t) devient inférieur au seuil critique 1/R₀, la croissance de I(t) ralentit et finit par décroître, même si R₀ > 1. C'est ce qui explique la forme caractéristique en cloche de l'épidémie : une croissance rapide suivie d'une décroissance progressive à mesure que l'immunité collective se développe.
2. Nullclines et points stationnaires [février 2025]
Nullclines
Les nullclines sont les courbes où les dérivées s'annulent. Pour le modèle SIR avec δ = μ :
Nullcline de I (dI/dt = 0) :
Nullcline de S (dS/dt = 0) :
_beta.0.7_gamma.0.2_mu.0.png)
Portrait de phase S-I : évolution de la fraction d'infectés en fonction des susceptibles
Points stationnaires
Deux types de points fixes :
- Point fixe sans maladie : (S*, I*, R*) = (1, 0, 0) (ou adapté selon μ, δ)
- Point fixe endémique : (S*, I*, R*) avec I* > 0 (apparaît quand R₀ > 1)
_beta.0.7_gamma.0.2_mu.0.png)
Champ de vecteurs montrant la direction de l'évolution du système
Interprétation des nullclines
- L'intersection des nullclines donne les points d'équilibre du système
- La nullcline de I est une verticale : seuil critique de susceptibles
- En dessous de ce seuil (S < S_nc), I diminue
- Au-dessus (S > S_nc), I augmente (si I > 0)
3. Modèle SIR sans naissance/mort [février 2025]
Dans le cas sans dynamique de population (μ = δ = 0), le modèle se simplifie :
Condition de prolifération
Pour que la maladie se propage, il faut dI/dt > 0, soit :
La maladie ne peut proliférer que si la fraction de susceptibles est suffisamment élevée.
Relation implicite S-R
En divisant l'équation de S par celle de R :
Cette équation se résout facilement :
avec S(0) = 1 (initialement, personne n'est immunisé).
_beta.0.7_gamma.0.2_mu.0.png)
Relation implicite entre susceptibles et retirés : S = exp(-R₀·R)
Solution stationnaire
À l'équilibre (t → ∞), I* = 0 et S* + R* = 1, d'où l'équation implicite :
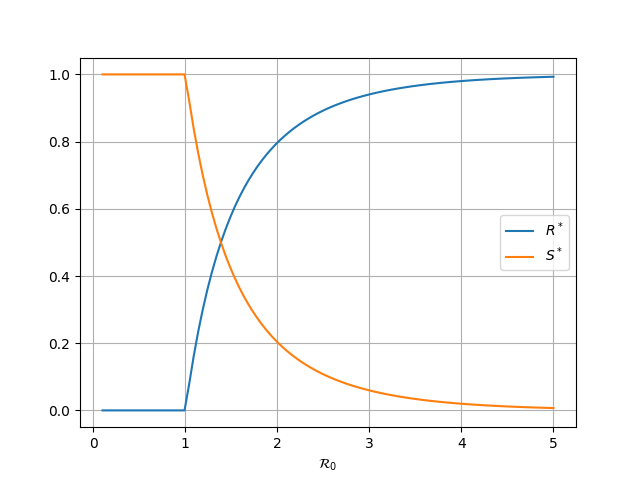
La résolution de cette équation donne la fraction finale de la population touchée par l'épidémie.

Fraction finale de la population touchée par l'épidémie en fonction de R₀
Exemple numérique
- R₀ = 3.5
- τ = 5 jours → γ = 0.2 jour⁻¹
- β = R₀ × γ = 0.7 jour⁻¹
- État stationnaire : S* = 0.034, I* = 0, R* = 0.966
- Interprétation : 96.6% de la population sera touchée par l'épidémie
_beta.0.7_gamma.0.2_mu.0.png)
Trajectoire du système dans le plan infectés-retirés
4. Modèle SIR avec naissance et mort [février 2025]
L'introduction d'une dynamique de population (μ > 0, δ = μ) maintient la population totale constante mais permet un renouvellement des susceptibles par naissance.
Paramètres
- R₀ = 3.5
- γ = 0.2 jour⁻¹ (τ = 5 jours)
- β = 0.7 jour⁻¹
- μ = δ = 0.02 jour⁻¹ (taux de natalité/mortalité)
Nouveau point fixe endémique
Contrairement au cas sans naissance/mort, le système converge vers un point fixe endémique avec I* > 0 :
_beta.0.7_gamma.0.2_mu.0.02.png)
Modèle avec dynamique de population : apparition d'un point fixe endémique non nul
Comparaison des comportements
Sans naissance/mort
Extinction de la maladie
Avec naissance/mort
État endémique stable
Les naissances maintiennent un flux constant de nouveaux susceptibles, permettant à la maladie de persister dans la population. C'est typique des maladies endémiques comme la grippe saisonnière.
Vérification numérique
Après simulation jusqu'à t = 200 jours, les valeurs obtenues convergent bien vers le point fixe théorique :
5. Conclusion et perspectives [février 2025]
Résultats clés
L'analyse du modèle SIR met en évidence plusieurs résultats fondamentaux en épidémiologie mathématique :
- Seuil épidémique : R₀ > 1 est nécessaire pour qu'une épidémie se propage
- Immunité collective : lorsque la fraction de susceptibles descend en dessous de 1/R₀, l'épidémie régresse
- Taille finale : donnée par l'équation implicite 1 - exp(-R₀ R*) - R* = 0
- Endémie : avec renouvellement de la population, la maladie peut persister indéfiniment
Extensions possibles du modèle
Le modèle SIR de base peut être enrichi pour représenter des situations plus complexes :
SEIR
Ajout d'un compartiment E (Exposed) pour les individus en période d'incubation
SIRS
Perte de l'immunité : retour des guéris vers le compartiment susceptible
Structuré par âge
Taux de contact et de mortalité dépendant de l'âge
Mobilité spatiale
Propagation géographique de la maladie (modèles méta-population)
Applications concrètes
Ces modèles sont utilisés quotidiennement par les agences de santé publique pour :
- Prévoir l'évolution des épidémies (grippe, COVID-19, Ebola...)
- Évaluer l'impact des mesures de contrôle (confinement, vaccination)
- Optimiser l'allocation des ressources (lits d'hôpital, vaccins)
- Déterminer les seuils de vaccination pour l'immunité collective